一.实验目的
1、用滴定法测定镀Ni、镀Cu溶液中主盐金属离子的含量;
2、用XRF荧光光谱仪测定镀Ni、镀Cu溶液中主盐金属离子的含量;
3、对两种方法测定的主盐离子含量进行比较,比较两者误差,以判定XRF仪器准确性。
4、对镀液进行加标,分别用两种方法测定其加标回收率并进行对比。
二.实验方法
(1)镀液配制:
电镀Ni溶液:选择普通镀镍液配方。六水合硫酸镍预先烘干至无水硫酸镍,称取硫酸镍(NiSO4) 80g,氯化钠(NaCl) 4g,硼酸(H3BO3) 33g,无水硫酸钠(Na2SO4) 30g,十二烷基硫酸钠(C12H25SO4Na) 0.05g。分别用热水溶解,混合在一个容器中,加水稀释到所需体积,静置澄清,用虹吸法或过滤法把镀液引入镀槽,再加入已经溶解的十二烷基硫酸钠溶液;搅拌均匀,配制成1000mL镀液取样分析。
电镀Cu溶液:选择普通镀铜液配方。五水合硫酸铜预先烘干至无水硫酸铜,称取硫酸铜(CuSO4) 50g,先将称取的硫酸铜溶解在配制体积三分之二的温水中,当硫酸铜完全溶解溶液和冷却后,在不断搅拌下慢慢地加入硫酸(H2SO4) 40mL(加入硫酸时为放热反应),配制成1000mL的溶液,静置溶液并进行过滤,对镀液进行取样分析。
(2)EDTA标准溶液的配制与标定:
0.05M EDTA溶液的配制:称取20g乙二胺四乙酸二钠溶于1L蒸馏水中,摇匀。
EDTA标准溶液的标定:称取于800°C灼烧至恒重的基准氧化锌1g (称准至0.2mg),用少许蒸馏水湿润,加盐酸溶液(1:1)至样品溶解,移入250ml容量瓶中,稀释至刻度,摇匀。取上述溶液20.00ml,加80m|水,用10%氨水中和至PH为7~8,加5ml氨-氯化铵缓冲溶液(PH=10),加5滴0.5%铬黑T指示剂,用0.05M EDTA溶液滴定至溶液由紫色变为纯兰色。
(3)溶液分析:
滴定法(TM)
测定Ni2+含量时用移液管吸取溶液10毫升,置于100毫升容量瓶中,加水至刻度,摇匀,吸取稀释液10毫升置于250毫升锥形瓶中,加氟化钾1克,摇晃至氟化钾溶解,再加水30毫升,此时溶液应呈浑浊,有微小的氟化镁沉淀生成,加pH=10缓冲液10毫升及紫脲酸铵指示剂少量,用0.05M EDTA溶液滴定由黄色变为紫红色为终点。滴定结果记录于表1-1中。
测定Cu2+含量时用移液管吸取镀液2毫升于500毫升锥形瓶中,滴加过氧化氢8滴,加水50毫升、煮沸一下,冷却,加水150毫升,氟化铵1克及三乙醇胺6滴,加氨水至溶液呈淡蓝色,加PAN 10~12滴,用0.050M EDTA溶液滴定至绿色为终点。滴定结果记录于表1-2中。
荧光光谱法(XRF)

本实验基于西凡仪器P1镀层测厚仪,该仪器可以支持镀层厚度检测、成分分析以及离子浓度分析。该设备采用智能基本参数法算法,并使用定制的液体测试杯。
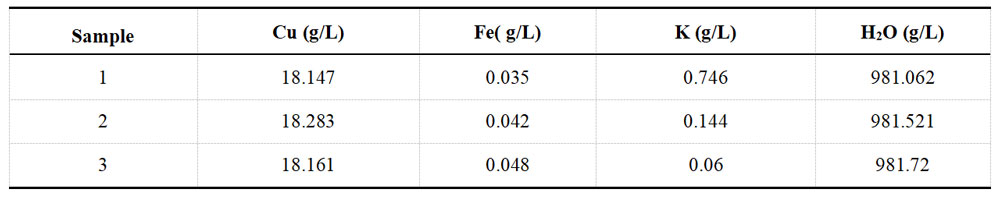
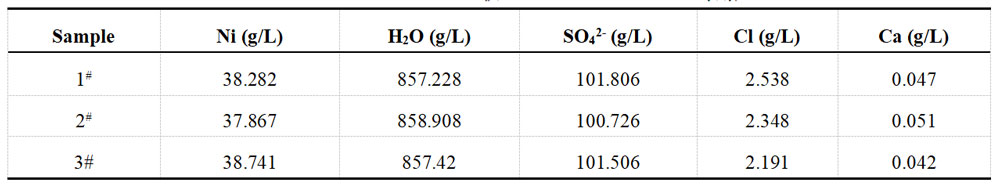
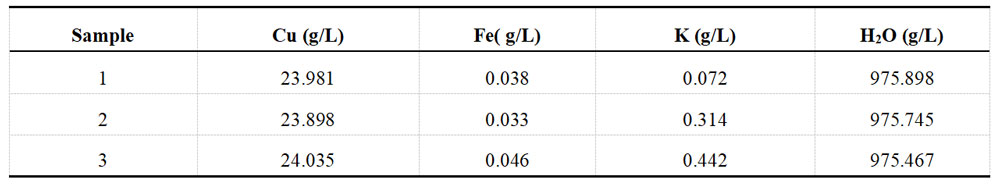
每组镀液另取部分样品,借助于XRF荧光光谱仪对其溶液中的离子进行测定,每组样品分别测定三次,镀Ni液和镀Cu液的测定结果分别记录于表1-3和表1-4中。
表1-1 酸性镀Ni液加标前Ni2+滴定数据
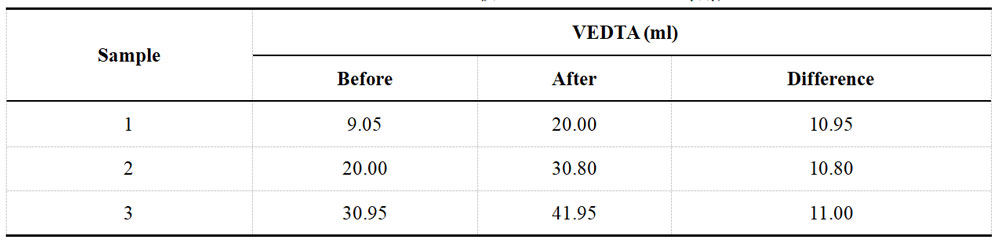
表1-2 酸性镀Cu液加标前Cu2+滴定数据
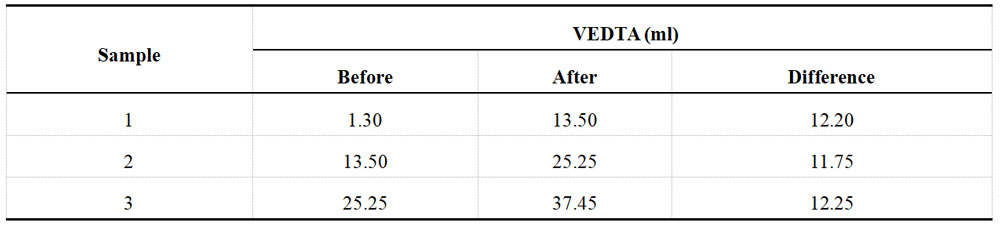
表1-3 酸性镀Ni液加标前 XRF测定数据
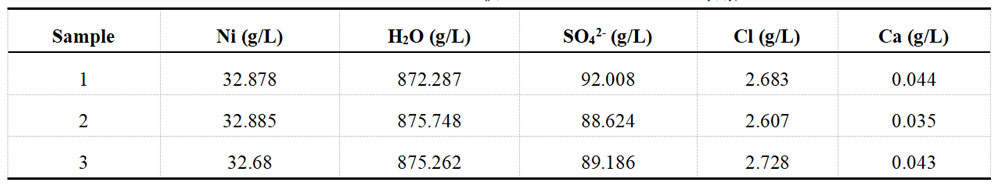
表1-4 酸性镀Cu液加标前 XRF测定数据
(4)加标回收:
加标前后镀液中硫酸镍浓度为100g/L和115g/L,硫酸镍的加标量为15g/L,相当于添加了5.691g/L的Ni2+。再次用0.05M EDTA溶液滴定,结果如表1-5所示。XRF测试结果如表1-6所示。
表1-5 酸性镀Ni液加标后Ni2+滴定
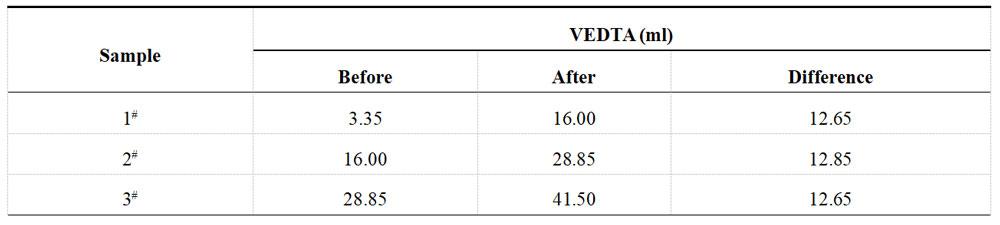
表1-6 酸性镀Ni液加标后 XRF测定数据
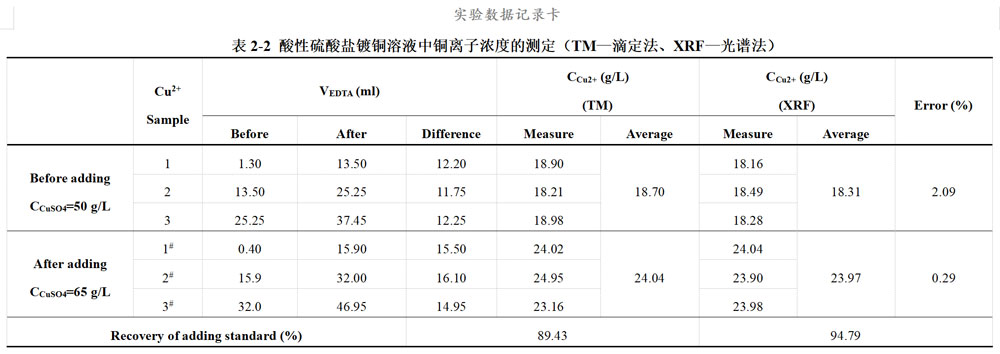
加标前后镀液中硫酸铜浓度为50g/L和65g/L,硫酸铜的加标量为15g/L,相当于添加了5.971g/L的Cu2+。再次用0.05M EDTA溶液滴定,结果如表1-7所示。XRF测试结果如表1-8所示。
表1-7 酸性镀Cu液加标后Cu2+滴定
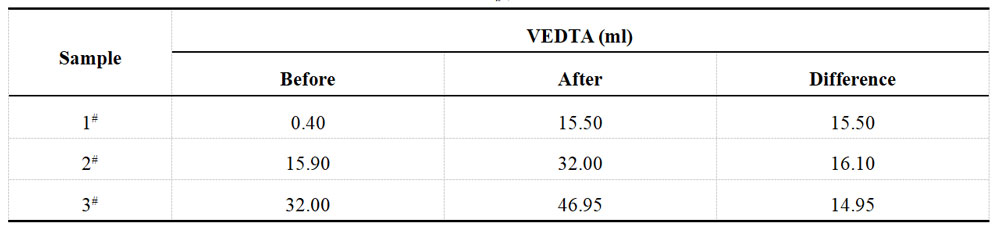
表1-8 酸性镀Cu液加标后 XRF测定数据
三.数据计算
(1)滴定法测定离子含量
镍离子含量的计算式:
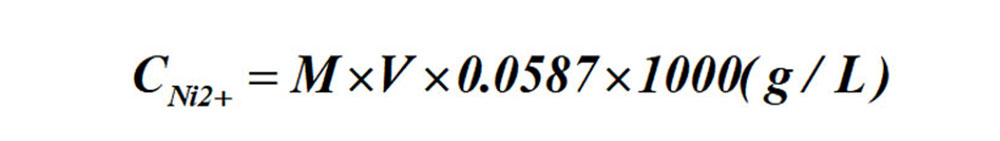
式中 M——标准EDTA溶液的克分子浓度;
V——耗用标准EDTA溶液的毫升数。
铜离子含量的计算式:
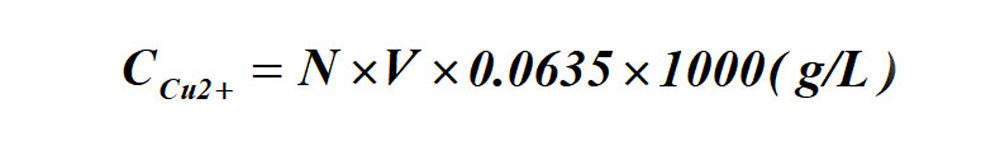
式中 N——标准EDTA溶液的当量浓度;
V——耗用标准EDTA溶液的毫升数。
(2)XRF与滴定法的测定误差
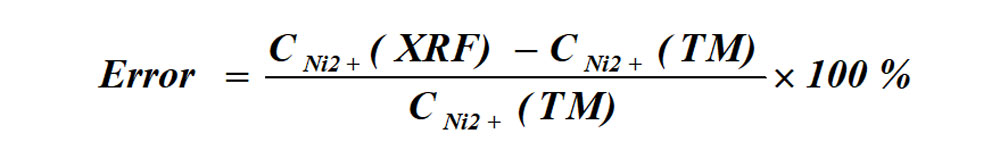
(3)加标回收率
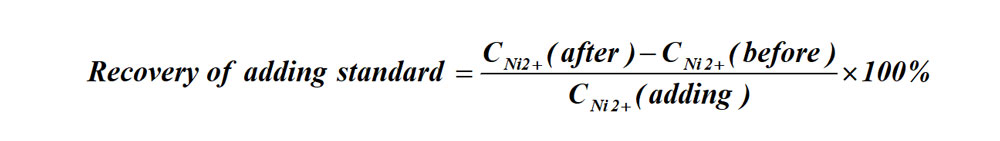
所有计算数据统一记录在数据卡的表2-1和表2-2中。
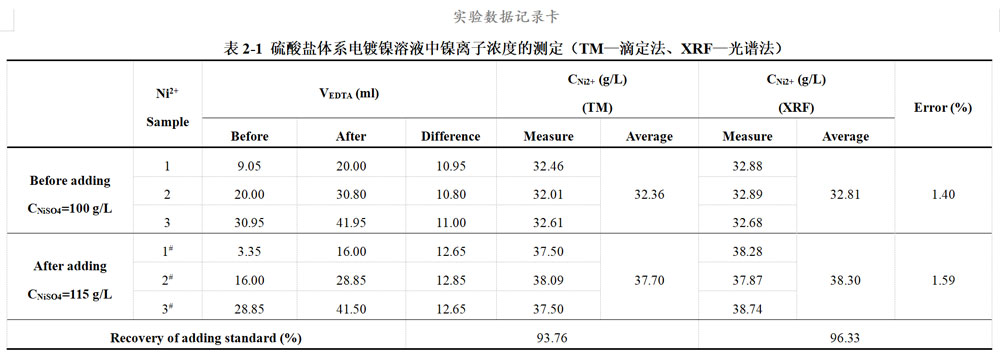
本实验电镀镍溶液选择传统酸性镀镍液(主要成分为硫酸镍和硼酸),加标前后镀液中硫酸镍(经烘干,不含结晶水)含量为100g/L和115g/L。硫酸镍的加标量为15g/L,相当于添加了5.691g/L的Ni2+。
Ni2+滴定所采用的标准溶液为0.050M的EDTA溶液,经标定后测得其实际量浓度为0.0505mol/L。
滴定法测定镍离子含量的计算式:
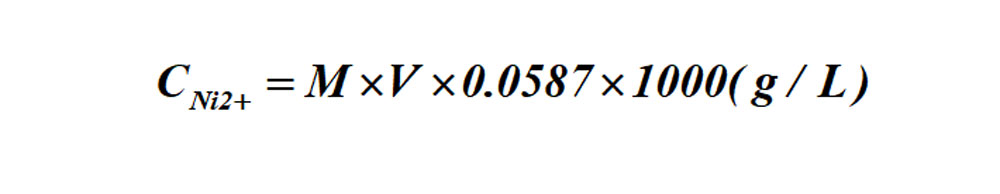
式中 M——标准EDTA溶液的克分子浓度;
V——耗用标准EDTA溶液的毫升数。
XRF仪器测定与滴定法测定误差的计算式;
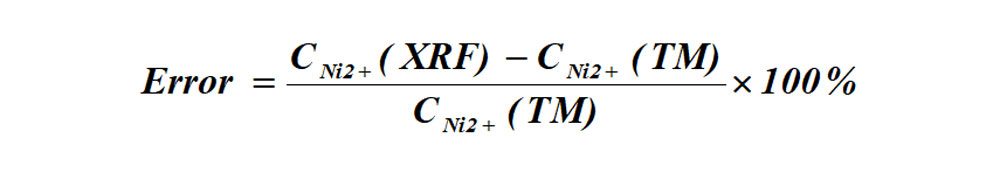
加标回收率的计算式:
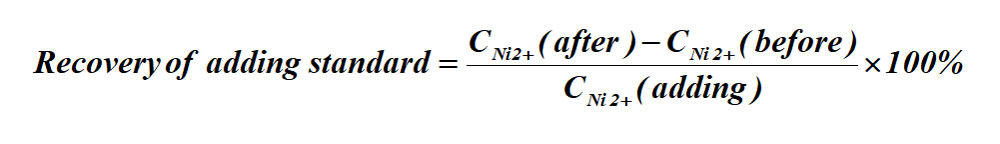
本实验电镀铜溶液选择传统酸性硫酸铜液(主要成分为硫酸铜和硫酸),加标前后镀液中硫酸铜(经烘干,不含结晶水)含量为50 g/L和65 g/L。硫酸铜的加标量为15 g/L,相当于添加了5.971 g/L的Cu2+。 Cu2+滴定所采用的标准溶液为0.050M的EDTA溶液,经标定后测得其实际量浓度为0.0488mol/L。
滴定法测铜镍离子含量的计算式:
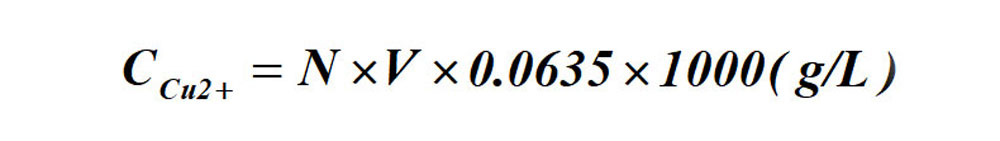
式中 N——标准EDTA溶液的当量浓度;
V——耗用标准EDTA溶液的毫升数。
XRF仪器测定与滴定法测定误差的计算式;
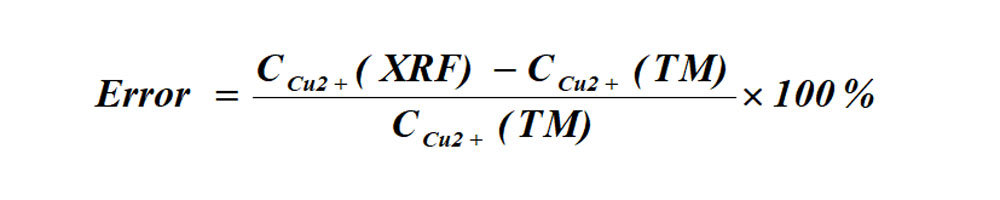
加标回收率的计算式:
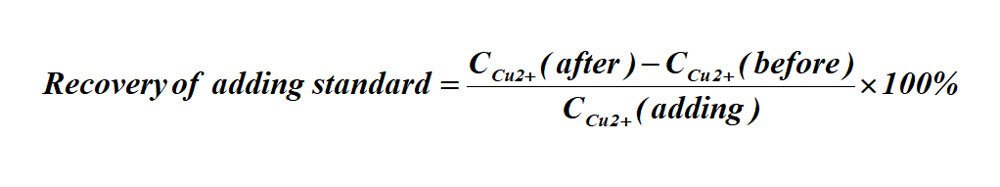
四.实验结果分析
如表2-1和表2-2中结果所示:
(1)滴定法与XRF的测试结果对比,两种方法的误差(Error)在0.29~2.09%的范围内。
(2)XRF较滴定法计算所得到的加标回收率(Recovery of adding standard)更接近于,主要是因为由于滴定法的读数误差、实验操作误差和对滴定终点判断的个体误差,使得滴定法测定的效果不如借助于荧光光谱仪。
(3)由于药品未完全烘干或烘干后容易吸收水分,使得测定的离子含量{CM2+(before)、CM2+(after)}低于理论值,同时作为理论计算值的CM2+(adding)不变而导致计算的加标回收率偏低(计算结果不高于)。同时由于滴定法和XRF采用的都是同一份样品,这一因素不会影响两种方法之间的比较。
根据数据卡中表2-1和表2-2的结果,绘制的对比分析图如图1所示。
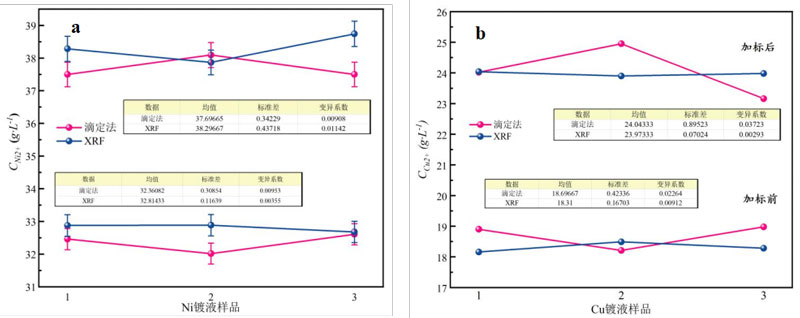
图1 加标前后滴定法与XRF测试结果对比图
(a.电镀Ni溶液,b.电镀Cu溶液)
图1中,均值用来表示不同方法测定的离子含量,标准差表示各数据样本的测试稳定程度,变异系数(=标准差/均值)表示基于样本本体量的测试误差程度。
如图1所示,可直观的看出:借助于滴定法测定离子含量,测试结果的波动比XRF法明显(即滴定法的标准差较大),这是由于存在溶液配制的差异、测量误差和操作人员的个体差异等,同时XRF法操作更简单,使得滴定法测定离子含量效果不如XRF。